O que é CRISPR Cas9
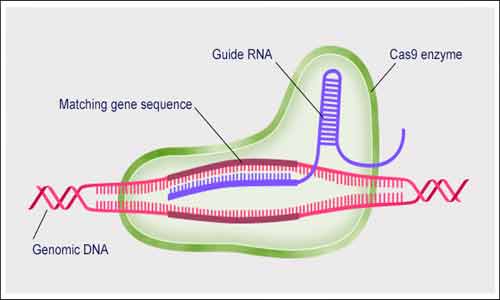
O que é CRISPR Cas9? Em português a sigla Cripr significa Repetições Palindrômicas Curtas Agrupadas e Regularmente Interespaçadas. A tecnologia CRISPR é uma ferramenta simples, porém poderosa, para a edição de genomas. Permite aos pesquisadores alterar facilmente as sequencias de DNA e modificar a função genética. Suas muitas aplicações potenciais incluem a correção de defeitos genéticos, o tratamento e a prevenção da propagação de doenças e a melhoria das culturas. No entanto, sua promessa também suscita preocupações éticas.
No uso popular, “CRISPR” (pronunciado “crisper”) é uma abreviatura para “CRISPR-Cas9”. CRISPRs são trechos especializados de DNA. A proteína Cas9 (ou “CRISPR-associado”) é uma enzima que age como um par de tesouras moleculares, capaz de cortar fios de DNA.

A tecnologia CRISPR foi adaptada dos mecanismos de defesa natural de bactérias e arqueias (o domínio de microorganismos unicelulares). Esses organismos usam ARN derivado de CRISPR e várias proteínas Cas, incluindo Cas9, para atacar ataques de vírus e outros corpos estranhos. Eles fazem isso principalmente cortando e destruindo o DNA de um invasor estrangeiro. Quando esses componentes são transferidos para outros organismos, mais complexos, permite a manipulação de genes ou “edição”.
CRISPR-Cas9: os principais jogadores
CRISPRs : “ CRISPR” significa “clusters de repetições palindrômicas curtas regularmente intercaladas”. É uma região especializada de DNA com duas características distintas: a presença de repetições de nucleotídeos e espaçadores. As sequências repetidas de nucleotídeos – os blocos de construção do DNA – estão distribuídas em toda a região de CRISPR. Os espaçadores são pedaços de DNA que são intercalados entre essas seqüências repetidas.
No caso das bactérias, os espaçadores são retirados de vírus que anteriormente atacaram o organismo. Eles servem como banco de memórias, o que permite que as bactérias reconheçam os vírus e combatem futuros ataques.
Isso foi demonstrado experimentalmente por Rodolphe Barrangou e uma equipe de pesquisadores da Danisco, uma empresa de ingredientes alimentícios. Em um artigo de 2007 publicado na revista Science, os pesquisadores usaram a bactéria Streptococcus thermophilus , que são comumente encontradas no iogurte e outras culturas leiteiras, como seu modelo. Eles observaram que após um ataque de vírus, novos espaçadores foram incorporados na região CRISPR. Além disso, a sequência de DNA destes espaçadores era idêntica a partes do genoma do vírus . Eles também manipularam os espaçadores removendo-os ou colocando novas seqüências de DNA viral. Desta forma, eles foram capazes de alterar a resistência das bactérias a um ataque por um vírus específico. Assim, os pesquisadores confirmaram que CRISPRs desempenham um papel na regulação da imunidade bacteriana.
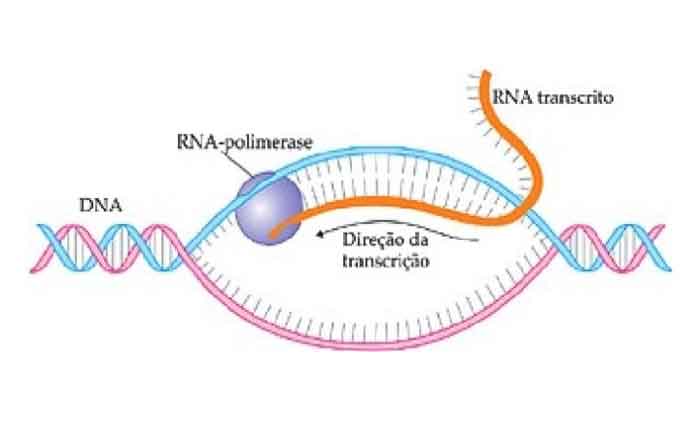
CRISPR RNA (crRNA): Uma vez que um espaçador é incorporado e o vírus ataca novamente, uma parte do CRISPR é transcrita e processada em CRISPR RNA, ou “crRNA”. A sequência de nucleótidos do CRISPR atua como um modelo para produzir uma sequência complementar de RNA de cadeia simples. Cada crRNA consiste em uma repetição de nucleotídeos e uma porção espaçadora, de acordo com uma revisão de 2014 de Jennifer Doudna e Emmanuelle Charpentier, publicada na revista Science.
Cas9: A proteína Cas9 é uma enzima que corta DNA estranho.
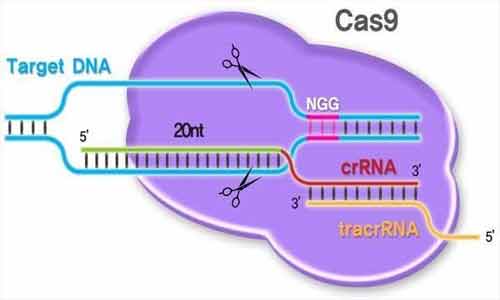
A proteína normalmente se liga a duas moléculas de ARN: crRNA e outro chamado tracrRNA (ou “CRRNA de trans-ativação”). Os dois, em seguida, guiam o Cas9 para o site alvo, onde ele fará seu corte. Esta extensão de DNA é complementar a um estiramento de 20 nucleótidos do crRNA.
Usando duas regiões separadas, ou “domínios” em sua estrutura, Cas9 corta os dois fios da dupla hélice do DNA, fazendo o que é conhecido como uma “ruptura de cadeia dupla”, de acordo com o artigo da Ciência 2014.
Existe um mecanismo de segurança incorporado, que garante que Cas9 não apenas corta em qualquer lugar em um genoma. As sequências de DNA curtas conhecidas como PAMs (“motivos adjacentes ao protospacer”) servem como etiquetas e ficam adjacentes à sequência de DNA alvo. Se o complexo Cas9 não vê um PAM ao lado de sua sequência de DNA alvo, ele não vai cortar. Esta é uma das possíveis razões pelas quais Cas9 nunca ataca a região CRISPR em bactérias, de acordo com uma revisão de 2014 publicada na Nature Biotechnology.
CRISPR-Cas9 como uma ferramenta de edição de genoma
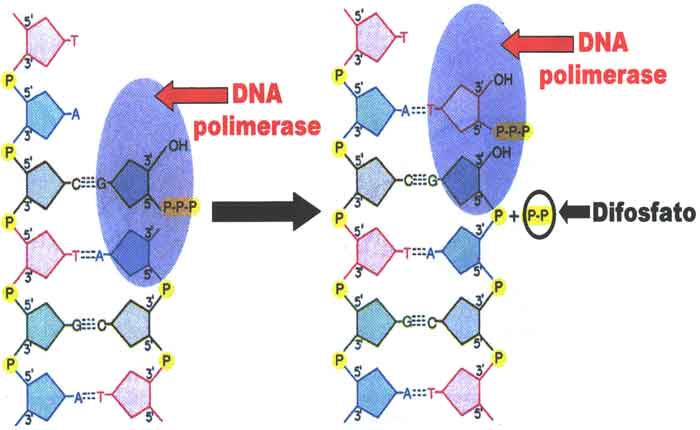
Os genomas de vários organismos codificam uma série de mensagens e instruções dentro de suas seqüências de DNA. A edição do genoma envolve a mudança dessas seqüências, alterando assim as mensagens. Isso pode ser feito inserindo um corte ou quebra no DNA e enganando os mecanismos naturais de reparo do DNA de uma célula para introduzir as mudanças que se quer. CRISPR-Cas9 fornece um meio para fazê-lo.
Em 2012, foram publicados dois trabalhos de pesquisa fundamentais nas revistas Science e PNAS , que ajudaram a transformar o CRISPR-Cas9 bacteriano em uma ferramenta simples e programável de edição de genoma.
Os estudos, conduzidos por grupos separados, concluíram que Cas9 poderia ser direcionado para cortar qualquer região do DNA. Isto poderia ser feito simplesmente mudando a sequência de nucleotídeos do crRNA, que se liga a um alvo de DNA complementar. No artigo da Ciência de 2012, Martin Jinek e colegas simplificaram ainda mais o sistema ao fundir o crRNA e o traRRNA para criar um único “RNA guia”. Assim, a edição do genoma requer apenas dois componentes: um RNA guia e a proteína Cas9.
“Operacionalmente, você projeta um trecho de 20 pares de bases [nucleotídeos] que combinam um gene que você quer editar”, disse George Church , professor Robert Winthrop de Genética na Harvard Medical School. É construída uma molécula de ARN complementar aos 20 pares de bases. A Igreja enfatizou a importância de garantir que a seqüência de nucleotídeos seja encontrada apenas no gene alvo e em nenhum outro lugar do genoma. “Então, o RNA mais a proteína [Cas9] vai cortar – como um par de tesouras – o DNA nesse site e, de modo ideal, em nenhum outro lugar”, explicou.
Uma vez que o DNA é cortado, os mecanismos de reparação natural da célula chutam e trabalham para introduzir mutações ou outras alterações no genoma. Há duas maneiras pelas quais isso pode acontecer. De acordo com o Huntington’s Outreach Project em Stanford (Universidade), um método de reparação envolve a colagem dos dois cortes juntos. Este método, conhecido como “união final não homóloga”, tende a introduzir erros. Os nucleotídeos são acidentalmente inseridos ou excluídos, resultando em mutações , o que pode interromper um gene. No segundo método, a quebra é corrigida preenchendo a lacuna com uma sequência de nucleotídeos. Para fazer isso, a célula usa um fio curto de DNA como um modelo. Os cientistas podem fornecer o modelo de DNA de sua escolha, escrevendo assim – em qualquer gene que desejam, ou corrigindo uma mutação.
Utilidade e limitações
CRISPR-Cas9 tornou-se popular nos últimos anos. A Igreja observa que a tecnologia é fácil de usar e é cerca de quatro vezes mais eficiente do que a melhor ferramenta de edição do genoma ( TALENS ).
Em 2013, pesquisadores dos laboratórios da Igreja e Feng Zhang do Broad Institute do Massachusetts Institute of Technology e Harvard publicaram os primeiros relatórios sobre o uso de CRISPR-Cas9 para editar células humanas em um cenário experimental . Estudos utilizando modelos in vitro (laboratório) e animais de doenças humanas demonstraram que a tecnologia pode ser efetiva na correção de defeitos genéticos. Exemplos de tais doenças incluem fibrose cística, catarata e anemia de Fanconi , de acordo com um artigo de revisão de 2016 publicado na revista Nature Biotechnology. Esses estudos abrem caminho para aplicações terapêuticas em seres humanos.
A tecnologia CRISPR também foi aplicada nas indústrias alimentar e agrícola para engenharia de culturas probióticas e para vacinar culturas industriais (para iogurte, por exemplo) contra vírus. Também está sendo usado em culturas para melhorar o rendimento, tolerância à seca e propriedades nutricionais.
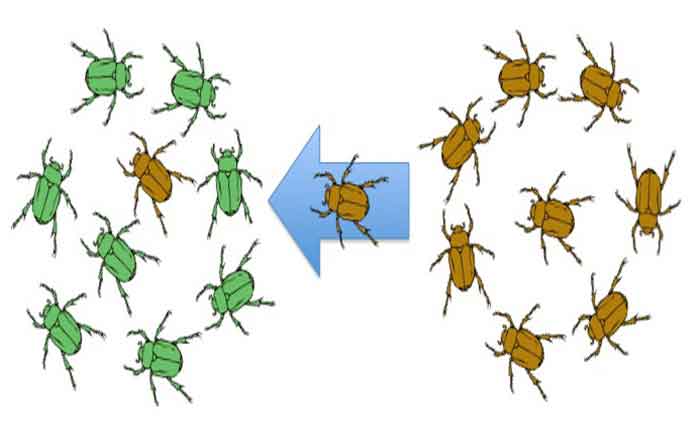
Uma outra aplicação potencial é criar unidades de genes. Estes são sistemas genéticos, que aumentam as chances de uma característica particular passando do pai para a prole. Eventualmente, ao longo das gerações, a característica se espalha por populações inteiras, de acordo com o Instituto Wyss . Os movimentos de genes podem ajudar a controlar a propagação de doenças como a malária, aumentando a esterilidade entre o vetor da doença – mosquiteiros femininos Anopheles gambiae – de acordo com o artigo 2016 Nature Biotechnology. Além disso, as unidades de genes também podem ser usadas para erradicar espécies invasivas e reverter a resistência a pesticidas e herbicidas , de acordo com um artigo de Kenneth Oye, de 2014, publicado na revista Science.
No entanto, CRISPR-Cas9 não está sem suas desvantagens.
“Eu acho que a maior limitação do CRISPR é que não é 100% eficiente”, disse Church à Live Science. Além disso, as eficiências de edição do genoma podem variar. De acordo com o artigo de Cielo 2014 de Doudna e Charpentier, em um estudo realizado em arroz, a edição de genes ocorreu em quase 50% das células que receberam o complexo Cas9-RNA. Considerando que, outras análises mostraram que, dependendo do alvo, as eficiências de edição podem atingir 80% ou mais.
Há também o fenômeno de “efeitos fora do alvo”, onde o DNA é cortado em locais que não o alvo pretendido. Isso pode levar à introdução de mutações não intencionais. Além disso, Church observou que mesmo quando o sistema corta o alvo, há uma chance de não conseguir uma edição precisa. Ele chamou esse “vandalismo do genoma”.
Limites de definição
As muitas aplicações potenciais da tecnologia CRISPR levantam questões sobre os méritos éticos e as conseqüências da adulteração de genomas.
No artigo da Ciência 2014, Oye e colegas apontam para o potencial impacto ecológico do uso de unidades de genes. Uma característica introduzida poderia se espalhar além da população alvo para outros organismos através do cruzamento. As unidades de genes também podem reduzir a diversidade genética da população alvo.
Fazer modificações genéticas para embriões humanos e células reprodutivas, como esperma e ovos, é conhecida como edição germinal. Uma vez que as alterações a estas células podem ser transmitidas para as gerações subsequentes, a utilização da tecnologia CRISPR para fazer alterações na linha germinal levantou uma série de preocupações éticas.
A eficácia variável, os efeitos fora do alvo e as edições imprecisas representam riscos de segurança. Além disso, há muito que ainda é desconhecido para a comunidade científica. Em um artigo de 2015 publicado na Science, David Baltimore e um grupo de cientistas, especialistas em ética e jurídicos observam que a edição germinal levanta a possibilidade de conseqüências não intencionais para as gerações futuras “porque há limites para o nosso conhecimento de genética humana, interações gênero-ambiente, e os caminhos da doença (incluindo a interação entre uma doença e outras condições ou doenças no mesmo paciente) “.
Outras preocupações éticas são mais matizadas. Devemos fazer mudanças que possam afetar fundamentalmente as gerações futuras sem ter seu consentimento? E se o uso da edição de linha germinativa virar ser uma ferramenta terapêutica para uma ferramenta de aprimoramento para várias características humanas?
Para resolver essas preocupações, as Academias Nacionais de Ciências, Engenharia e Medicina juntaram um relatório abrangente com diretrizes e recomendações para a edição do genoma.
Embora as Academias Nacionais exijam cautela na busca da edição da linha germinal, eles enfatizam que “cautela não significa proibição”. Eles recomendam que a edição da linha germinal seja feita somente em genes que levem a doenças graves e somente quando não há outras alternativas de tratamento razoáveis. Entre outros critérios, eles enfatizam a necessidade de ter dados sobre os riscos e benefícios para a saúde e a necessidade de supervisão contínua durante os ensaios clínicos. Eles também recomendam o acompanhamento das famílias por várias gerações.

Em algum momento poderemos todos termos pele em tom verde para sintetizarmos fotossíntese e viver de luz, seremos seres de luz… verdes
Ah vai da o cu seu arrobado, fila da puta, ta falando de coisa certa que é o futuro ai você vem com essa babaquices de corno, ai falando de pele verde e fotossíntese..
Pra que essa agressividade toda. Vai que pele verde pra realizar fotossintese é o futuro, e o nivaldo está à frente do seu tempo.
ah da uma sugada aqui o mal educado